2018 年 9 月 25 日,广州—— 我国首个获批上市的细胞周期蛋白依赖性激酶 CDK4/6 抑制剂爱博新 ®IBRANCE®(哌柏西利, palbociclib)于 9 月 25 日在广州开出全国首日处方。中山大学肿瘤医院、广东省人民医院、中山大学孙逸仙纪念医院、广东省中医院和中山大学附属第一医院等五家医院为乳腺癌晚期患者开出 CDK4/6 抑制剂处方,正式开启我国晚期乳腺癌治疗「CDK4/6 激酶抑制剂与内分泌治疗」联合用药时代。这也标志着我国激素受体阳性(HR+)人表皮生长因子受体 2 阴性(HER2-)晚期乳腺癌治疗领域结束了近十年来没有突破性创新疗法的局面。

图 1: 中山大学肿瘤医院内科乳腺病区王树森主任在广州开出全国首日处方
爱博新 ®是由辉瑞研发的全球首个用于治疗激素受体(HR)阳性、人表皮生长因子受体 2(HER2)阴性的局部晚期或转移性乳腺癌的 CDK4/6 抑制剂,应与芳香化酶抑制剂联合使用作为绝经后女性患者的初始内分泌治疗,于今年 7 月 31 日在中国获批。这一创新药物将为 HR+/HER2-晚期乳腺癌患者提供创新的治疗选择,显著延长患者的无进展生存期,改善她们的生活质量,同时也将造福于患者家庭和社会。

图 2: 广东省人民医院肿瘤中心乳腺科廖宁主任在广州开出全国首日处方
全球首个 CDK4/6 的选择性抑制剂,有效延长 10 个月中位无进展生存期
乳腺癌是严重威胁全世界女性健康的第一大恶性肿瘤。2015 年,中国新发乳腺癌病例达 27.2 万,死亡约 7 万余例。晚期乳腺癌的形势更为严峻,确诊的每 10 个患者就有 1 个为晚期。而且在接受过手术及规范治疗的早期乳腺癌患者中也有 30-40% 会发展为晚期乳腺癌。有别于早期乳腺癌治疗方式的多样化,近 10 年来我国晚期乳腺癌的治疗药物方面无重大进展,缺乏突破性创新疗法。晚期乳腺癌患者的总体中位生存期仅有 2-3 年,5 年生存率仅约 20%,迫切需要创新治疗方案。

图 3: 广东省人民医院肿瘤中心乳腺二科王坤主任在广州开出全国首日处方
全球注册研究显示,爱博新 ®联合来曲唑治疗激素受体(HR)阳性、人表皮生长因子受体-2(HER-2)阴性患者的中位无进展生存期长达 24.8 月,而单独接受来曲唑单药治疗患者的中位无进展生存期仅为 14.5 月。相比来曲唑单药,爱博新 ®联合来曲唑治疗显著延长了晚期乳腺癌患者 10 个月的中位无进展生存期。
爱博新 ®与内分泌治疗具有协同作用,上游和下游同时阻断 ER 通路
细胞周期蛋白依赖性激酶 4 和 6(CDK4/6),是细胞分裂周期的关键调节因素,能够驱动细胞分裂。CDK4/6 在许多癌症中均过度活跃表达,导致细胞分裂周期失控,是癌症的一个标志性特征。辉瑞公司推出的全球第一个周期蛋白依赖性激酶(CDK)4/6 的选择性抑制剂爱博新 ®,通过抑制 CDK4/6,恢复细胞周期控制,从而阻断肿瘤细胞增殖。
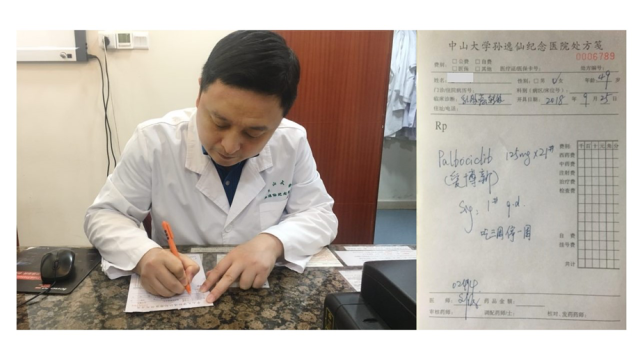
图 4: 中山大学孙逸仙纪念医院乳腺外科刘强主任在广州开出全国首日处方
爱博新 ®与内分泌治疗具有协同作用,共同阻断 ER 通路的上游和下游组件,抑制肿瘤细胞增殖:爱博新 ®联合内分泌治疗较内分泌单药可获得更强和持久的细胞周期阻滞作用,诱导细胞死亡和肿瘤缩小。

图 5: 广东省中医院乳腺科陈前军主任在广州开出全国首日处方
爱博新 ®将在全国 35 个城市陆续上市
2013 年美国食品与药品管理局(FDA)核准爱博新 ®为治疗晚期乳腺癌的突破性新药, 2015 年 FDA 以快速审批程序批准爱博新 ®上市,用于治疗晚期乳腺癌。基于此突破性进展,美国国立综合癌症网络(NCCN)指南推荐爱博新 ®联合芳香化酶抑制剂作为 HR+/ HER2-晚期或转移性乳腺癌的一线治疗方案。

图 6: 中山大学附属第一医院肿瘤科龙健婷主任在广州开出全国首日处方
截至目前,爱博新 ®已在全球 86 个国家和地区获批上市,中国是第 87 个。据悉,爱博新® 在继广州上市后,还将在北京、上海、成都、南京、杭州、沈阳等 35 个城市陆续上市。
